Presentazione
Precedente
- 2.4-
Alessandro Volta: la pila.
Volta occupa un posto molto
importante nella storia dell’elettrochimica per aver
costruito la famosa pila.
Le pile trasformano
spontaneamente l’energia chimica delle reazioni in energia
elettrica, sfruttando le reazioni di ossidoriduzioni. Come
conduttori vengono utilizzati i metalli, che avendo numerosi
elettroni in libero movimento, permettono appunto il passaggio di
corrente, mentre nei conduttori elettrolitici gli incaricati del
trasporto dell’elettricità sono gli ioni:
Positivi (cationi),
che si dirigono verso il polo negativo
Negativi (anioni), che si dirigono verso il polo positivo.
Gli elettrodi costituenti
le pile si realizzano immergendo un filo, una lamina o una barra
di metallo in una soluzione contenente ioni dello stesso metallo.
La pila di Volta (Fig. 1), fu realizzata con lastre di zinco (Zn),
fogli di feltro e lastre di rame (Cu). Il feltro viene bagnato
con una soluzione di acqua e sale.
| Un
altro tipo di cella voltaica relativamente semplice, è
la pila di Daniell, costituita da elettrodi di zinco e
rame, immersi in soluzioni dei rispettivi sali separati
da un setto poroso. Lo zinco dell’elettrodo se ne va
in soluzione, sotto forma di ioni Zn+2
lasciando nella barretta i suoi due elettroni: Polo (-)
Anodo Zn° - 2e -> Zn+2 Ossidazione |
| |
|

|
In
tale reazione si verifica il processo d’ossidazione
in cui il numero d’ossidazione dello zinco, passa da
0 a +2. Gli elettroni, attraverso il circuito esterno, si
trasferiscono alla barra di rame. La reazione al catodo
porta alla riduzione del rame che passa da Cu+2
a Cu°, acquistando elettroni e depositandoli sull’elettrodo.
Polo (+) Catodo Cu+2
+ 2e ->Cu° Riduzione
Questo tipo di pila
presenta una differenza di potenziale fra i due poli di 1,1
Volt. La reazione conclusiva si può riassumere come
segue:
|
Anodo (-) Zn° - 2e -> Zn+2
Ossidazione 1
Catodo (+) Cu+2 + 2e -> Cu° Riduzione 1
Zn° + Cu+2 à Zn+2 + Cu°
All’anodo si
verificano sempre reazioni di ossidazione, mentre al
catodo sempre di riduzione. Il voltaggio (in questo caso
di 1,1 V.) viene definito come differenza di potenziale (d.d.p.)
fra 2 elettrodi e può essere interpretata come la "pressione
" necessaria a spingere elettroni da un elettrodo
all’altro.
|
La pila di Daniell è così
costituita:
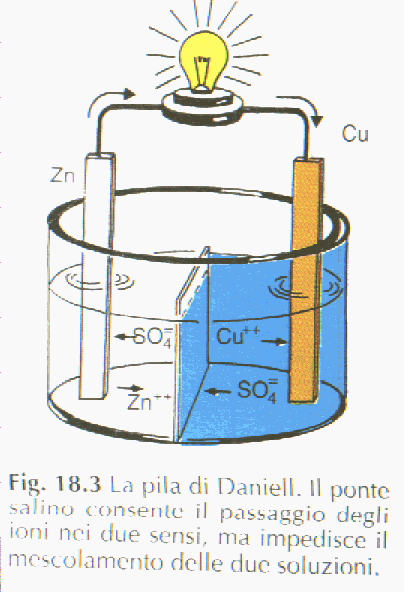 |
|
Per
stabilire quali fossero gli elementi in grado di
ossidarsi e quelli in grado di ridursi, bisognava
costruire una scala con un valido punto di riferimento.
Come tale si è scelto l’idrogeno (H).La scala dei potenziali
normale di riduzione (E°) è stata costruita misurando
il d.d.p. di una pila nella quale l’elettrodo a
idrogeno, (appositamente costruito, come riportato nella
figura seguente, dato che l’idrogeno si trova allo
stato gassoso), rappresenta un polo e l’elemento di
cui si vuol conoscere E°, l’altro polo.
|
Essendo E° (di H+1)
uguale a 0, il d.d.p che si legge sul voltometro, ci dà
direttamente il valore E° dell’altro elettrodo. La formula
impiegata per il calcolo è:
E° pila = E°
catodo – E° anodo
Non trovandosi allo stato
solido, l’elettrodo a idrogeno deve essere così costruito:
 |
|
Scala
potenziali di riduzione:
…..
…...
Sn+4
0,15 Si riduce
2H+1
0,00
Pb+2
-0,13 Si ossida
…..
……
|
Tutte le misure della scala
sono state fatte in condizioni standard (pressione, temperatura
di 25°C, concentrazione 1M).
In cima alla lista vi sono
i migliori ossidanti (quindi si riducono), in fondo i migliori
riducenti (si ossidano). La scala dei potenziali è fondamentale
per stabilire la spontaneità e il verso di una razione, nonché
per la progettazione di pile. Ogni reazione di ossidoriduzione può
essere divisa in due semireazioni:
Reazione di ossidazione ANODO
Reazione di riduzione CATODO
Per decidere quali delle
due semireazioni è di ossidazione e quale di riduzione, basta
vedere la scala, in cui il valore più alto di E° sta ad
indicare la riduzione della semireazione.
Nel corso del tempo le pile
sono diventate sempre più piccole, ma allo stesso tempo più
efficienti e affidabili. Tra le più importanti vi sono:
Pila a secco: tali
pile utilizzano lo zinco come agente riducente e MnO2
come ossidante. L’involucro esterno della pila è di zinco e
rappresenta l’anodo (-), mentre il catodo (+), è costituito
da un bastoncino di carbone che affonda nella "pasta"
umida di MnO2 e NH4Cl. Queste
pile sono abbastanza complicate ed hanno un d.d.p. di 1,5 V.
Pila alcalina: L’agente
riducente di questa pila è sempre lo zinco, mentre l’ossidante
è MnO2. L’unica cosa che variadalla precedente
pila è l’elettrolita, che non è più il cloruro di ammonio,
ma una soluzione acquosa di idrossido di potassio. Tali pile
hanno maggiore durata e maggiora stabilità di voltaggio.
Accumulatore a piombo:
Lo svantaggio della pila a secco è l’impossibilità di
ricaricarla. Gli accumulatori invece, possono una volta scaricati,
essere ricaricati.
| Le semireazioni
agli elettrodi sono le seguenti: Polo negativo Pb + SO4-2
- 2e à PbSO4
Polo positivo PbO2 + 4H+1 + SO4-2
+ 2e à PbSO4 + H2O
Pb + PbO2 + 4H+1 + 2SO4 -2
2PbSO4 + 2H2O
La d.d.p. tra una
coppia di elettrodi è di circa 2 V.
Le batterie delle automobili ne utilizzano dunque sei (che
generano in totale 12 V).
|
 |



